
24 juillet 2024

17 mai 2024
Pour qu’un générique soit autorisé, sa bioéquivalence doit notamment être démontrée. Cela signifie que la quantité et la vitesse à laquelle le corps absorbe la substance active doivent correspondre à l’original dans des limites strictes. Les fabricants doivent le prouver au moyen d’analyses. Cette procédure d’autorisation garantit que le générique possède la même qualité et la même sécurité. En outre, le fabricant doit prouver que la production est conforme aux normes de qualité, ce qui est vérifié par des contrôles aléatoires et des inspections des locaux. Les génériques sont donc tout à fait équivalents aux produits originaux en termes de qualité et de sécurité.
Les biosimilaires sont également autorisés selon les mêmes normes strictes de qualité, de sécurité et d’efficacité que tous les autres médicaments. Leur similitude avec le produit de référence doit être prouvée via les facteurs décisifs que sont la qualité, l’activité biologique, la sécurité et l’efficacité. L’autorisation de biosimilaires repose avant tout sur des études analytiques comparatives. Les fabricants doivent prouver que le médicament biosimilaire est suffisamment similaire à une «préparation de référence en termes de structure, de qualité pharmaceutique, d’activité biologique, d’efficacité, de sécurité et d’immunogénicité, afin d’exclure avec une certitude suffisante des différences cliniques pertinentes». Les méthodes analytiques et biotechnologiques les plus récentes sont utilisées pour démontrer la comparabilité avec les produits de référence.
Source: intergenerika.ch, biosimilar.ch
Quels sont les avantages des génériques et des biosimilaires?
Les génériques et les biosimilaires contribuent de manière significative aux économies de coûts dans le système de santé, car ils sont nettement moins chers que les préparations originales ou de référence. Cela est rendu possible par les coûts de recherche et de développement moindres des fabricants de génériques. L’utilisation de médicaments génériques permet aux systèmes de santé de réaliser des économies considérables, notamment en ce qui concerne les prescriptions à long terme pour les maladies chroniques.
Toutefois, en comparaison européenne, la Suisse est à la traîne en ce qui concerne les biosimilaires, et ce bien que les produits biopharmaceutiques modernes permettent des traitements et des guérisons dans des domaines thérapeutiques où il n’y avait guère de possibilités jusqu’à présent. Ils offrent ainsi aux patientes et patients concernés de nouvelles opportunités d’améliorer leur qualité de vie. Les biosimilaires sont une opportunité de réduire les coûts sans mettre en péril la sécurité des patients et patientes, la sécurité de l’approvisionnement ou l’accès à des traitements importants. Dans ce contexte, les biosimilaires sont indispensables pour rendre viables les innovations onéreuses dans le domaine des substances actives biologiques. Toutefois, la part encore faible de biosimilaires en Suisse n’est pas à la hauteur de leur importance thérapeutique. C’est pourquoi, ces derniers temps, l’OFSP s’engage davantage en faveur de la promotion des biosimilaires par le biais de différentes mesures.
Dans le plus grand assortiment pharmaceutique et non-pharma de Suisse, vous trouverez chez Galexis tous les médicaments RX et OTC enregistrés dans notre pays, dont un nombre croissant de biosimilaires.
Outre les avantages liés aux coûts, les génériques présentent d’autres caractéristiques positives qui les distinguent des préparations originales. Ils ne contiennent par exemple que des substances actives éprouvées qui sont parfaitement connues et documentées sur la base d’une longue expérience thérapeutique.
En outre, les génériques sont généralement des préparations plus modernes que leurs produits de référence développés il y a 10 ans ou plus, car les normes techniques de développement et de fabrication ont parfois évolué de manière significative. Les formes galéniques améliorées permettent notamment d’éviter les additifs tels que les conservateurs. Les génériques peuvent souvent être proposés sous des formes de traitements plus faciles à prendre, par exemple sous forme de comprimés sécables, véganes ou sans lactose.
Comment le marché des génériques et des biosimilaires est-il structuré?
Fondamentalement, le marché des médicaments est divisé en deux domaines: le marché des médicaments brevetés et le marché des médicaments non brevetés. Le marché des médicaments brevetés englobe les innovations, tandis que celui des médicaments non brevetés englobe les médicaments de substitution (génériques et biosimilaires) ainsi que les originaux non brevetés. Le marché des médicaments non brevetés est également appelé «marché des médicaments substituables», c’est-à-dire la partie du marché des médicaments dans laquelle une substitution de la préparation originale ou de référence par le générique ou le biosimilaire correspondant est possible. Le marché des médicaments brevetés et le marché des médicaments non brevetés représentent chacun environ la moitié du marché global en termes de chiffre d’affaires (fig. 1), tandis que le marché des médicaments non brevetés représente plus de 90% en termes de nombre de boîtes délivrées (fig. 2).
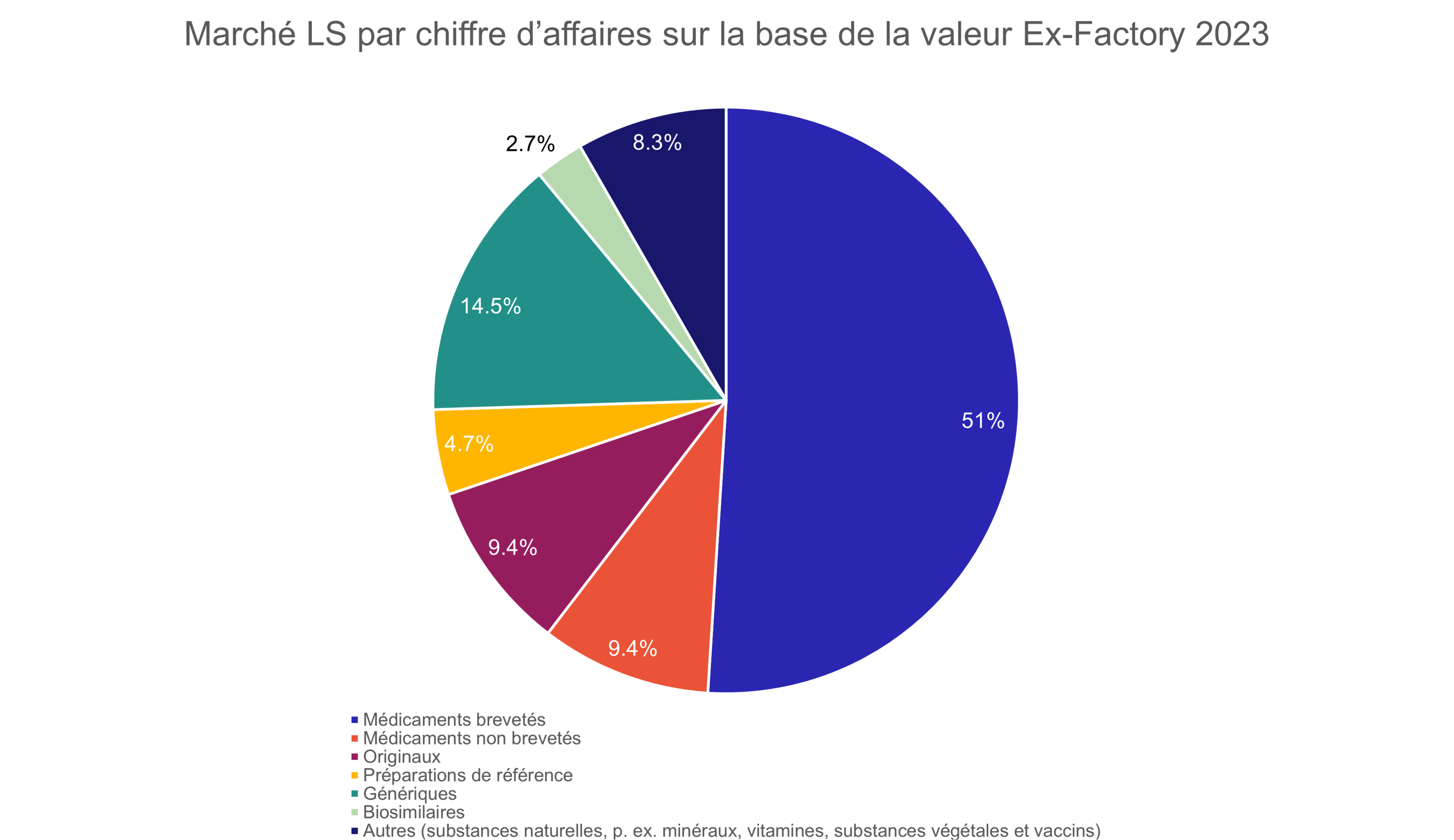
Le nombre de génériques et de biosimilaires qui pourraient en principe être disponibles dépend donc directement du nombre de médicaments originaux qui sont développés et dont les brevets arrivent à expiration. Plus la part des génériques sur le marché des médicaments substituables est importante par rapport aux originaux, plus le potentiel d’économie est exploité. Si l’on compare par exemple les génériques aux produits originaux pour 2023, on constate que davantage de génériques sont délivrés, tant en termes de chiffre d’affaires (14.5% contre 9.4% du marché global, fig. 1) qu’en boîtes (31.2% contre 17.6% du marché global, fig. 2). Les 9.4% (en chiffre d’affaires) et 17.6% (en boîtes) restants représentent le potentiel théorique de substitution par des génériques.
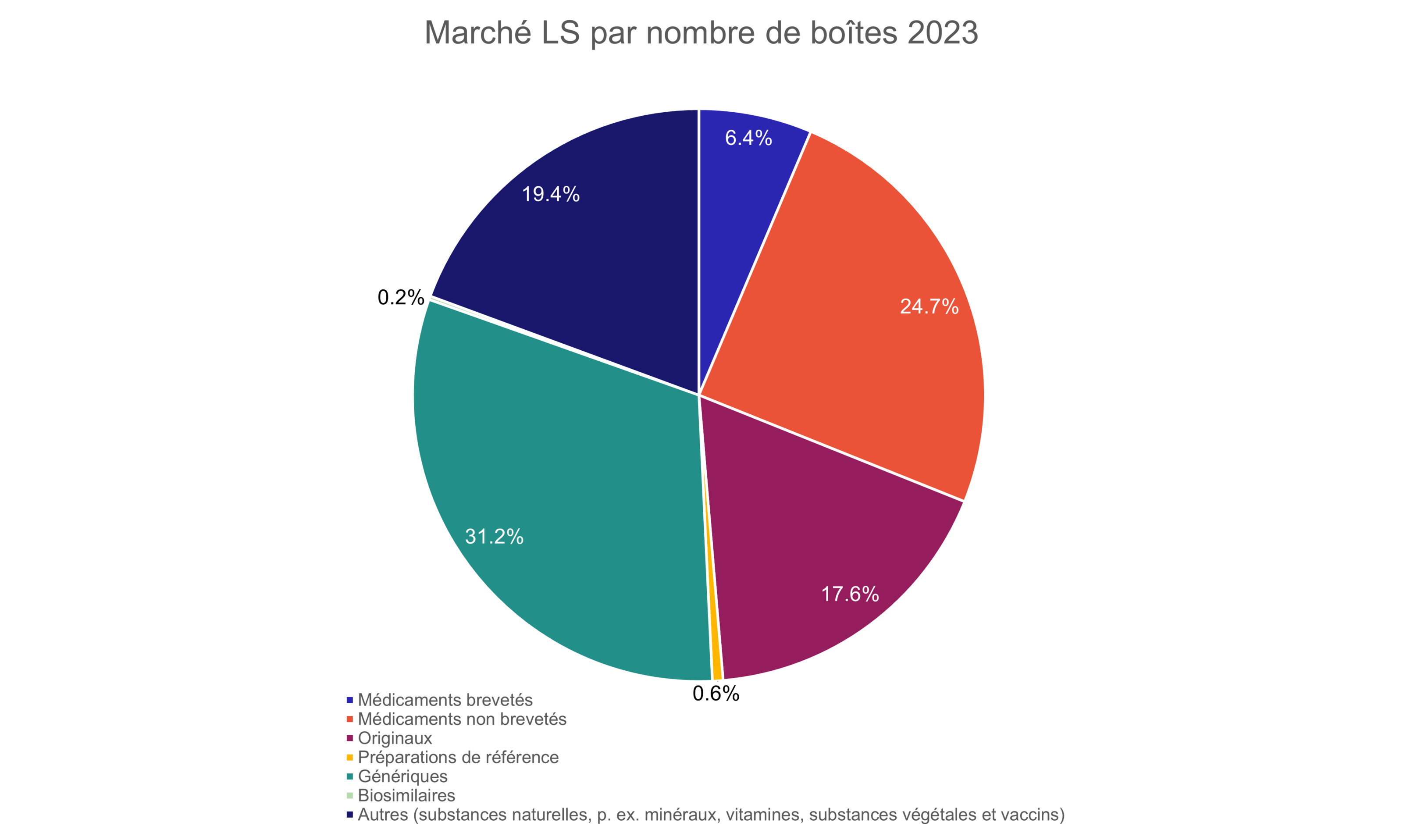
Les biosimilaires offrent toutefois un grand potentiel d’économies supplémentaires, comme le montrent les chiffres. Ainsi, en 2023, davantage de produits de référence (biosimilaires) ont été remis, tant en termes de chiffre d’affaires (4.3% vs 2.7% du marché global, fig. 1) qu’en termes de boîtes (0.6% vs 0.2% du marché global, fig. 2). Cela est d’autant plus important que de nombreux brevets de médicaments biologiques expireront au cours des prochaines années (voir aussi le paragraphe «Evolution du marché des génériques vers le marché des biosimilaires»).
Néanmoins, dès les premiers mois de l’année 2024, une forte dynamique de marché s’observe au sein du marché des médicaments substituables, en raison des différentes mesures de l’OFSP qui sont entrées en vigueur le 1er janvier et de celles qui entreront en vigueur le 1er juillet (voir également à ce sujet le paragraphe «Pourquoi cela vaut-il la peine?»). Ainsi, les chiffres d’affaires des génériques et des biosimilaires ont en partie nettement augmenté, tandis que l’utilisation des originaux ou des produits de référence a reculé. Cette tendance devrait se poursuivre au cours de l’année.
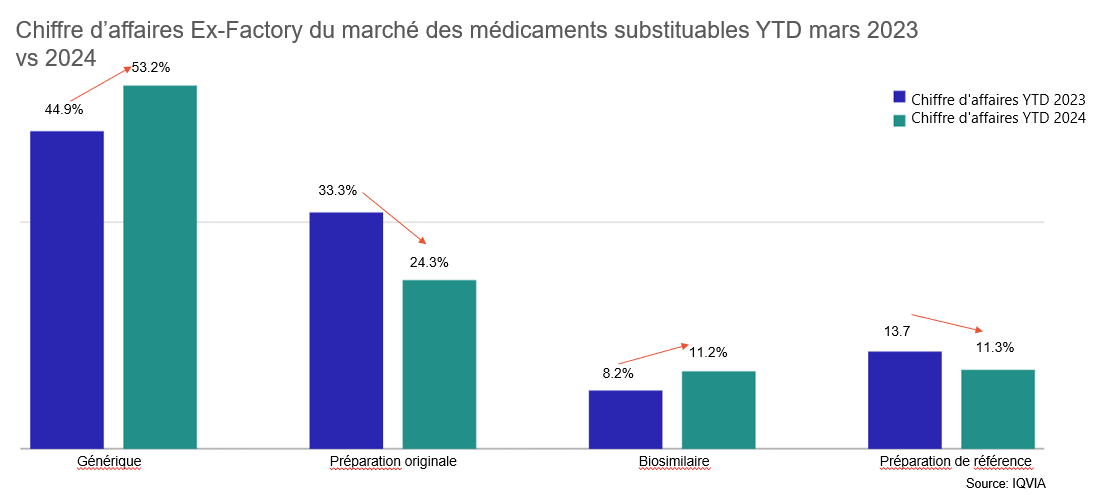
Evolution du marché des génériques vers le marché des biosimilaires
Pendant longtemps, le marché des médicaments substituables n’a pratiquement été qu’un marché de génériques. Jusqu’à récemment, la part du chiffre d’affaires des brevets arrivant à expiration pour les substances actives fabriquées selon un procédé chimique était nettement plus élevée que celle des substances actives fabriquées selon un procédé biologique. Le marché des médicaments substituables est toutefois soumis à une forte dynamique, ce qui laisse présager une évolution considérable des parts des génériques et biosimilaires dans les années à venir. La part des biomédicaments dont le brevet va expirer au cours des prochaines années a massivement augmenté et continuera de croître, car les médicaments biologiques occupent une place de plus en plus importante dans le traitement et la guérison de maladies pour lesquelles il n’existait auparavant aucune possibilité de traitement. Aujourd’hui déjà, le chiffre d’affaires mondial des biomédicaments dont le brevet est arrivé à expiration dépasse le chiffre d’affaires des synthétiques dont le brevet est arrivé à expiration (fig. 4).
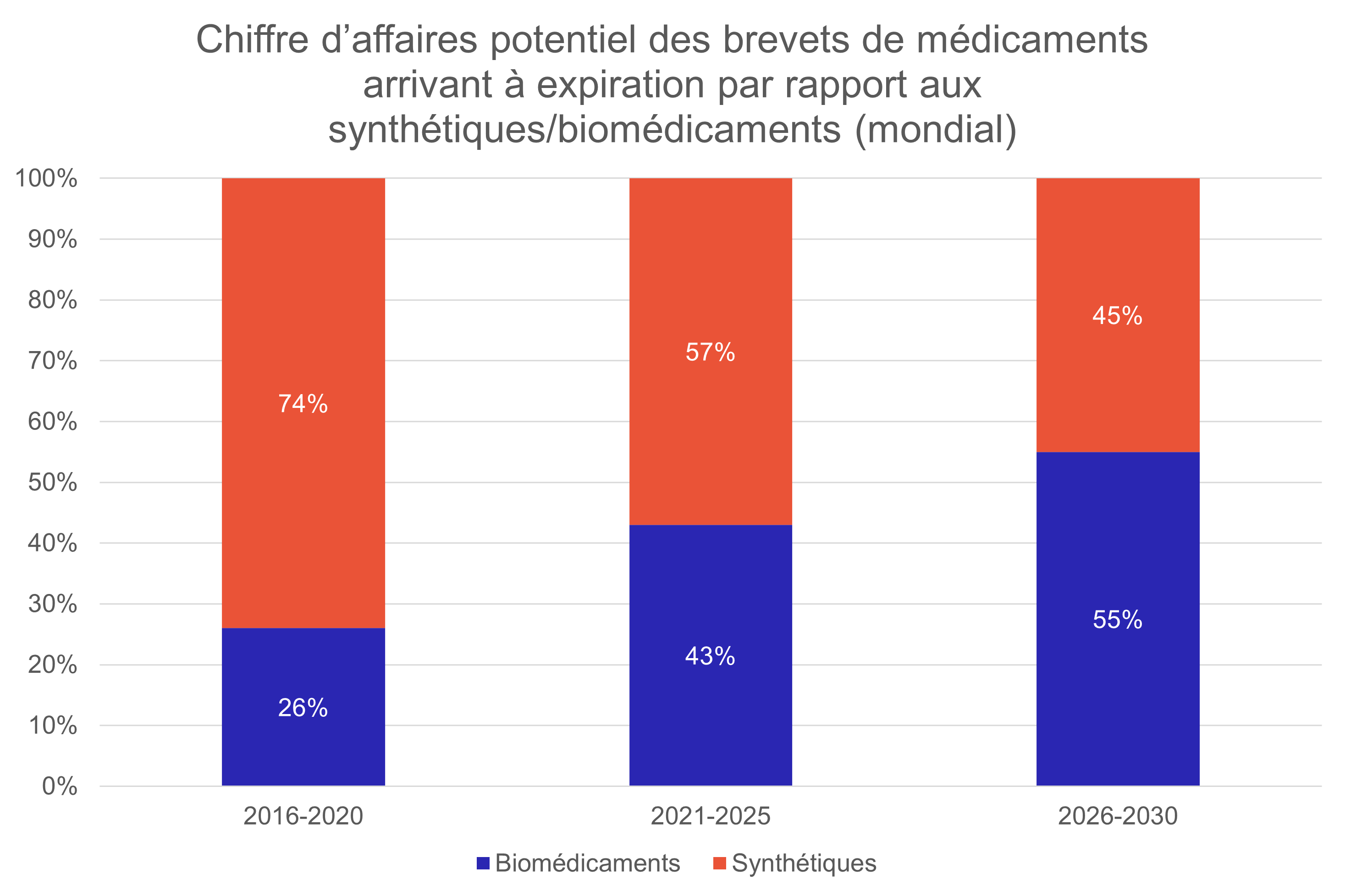
Les biosimilaires continueront donc de gagner en importance afin de maîtriser les coûts dans le système de santé sans compromettre la sécurité des patients et patientes, la sécurité de l’approvisionnement ou l’accès à des traitements importants. Parallèlement, le développement de biosimilaires contribue également à la viabilité financière de tels médicaments biologiques coûteux. Il est donc important de se préparer suffisamment tôt à cette évolution.
Quels sont les défis sur le marché des génériques et des biosimilaires?
Les génériques et les biosimilaires – bien que déjà nettement moins chers que les produits originaux ou de référence – sont soumis à une forte pression sur les coûts. Sur le marché suisse de la santé, fortement réglementé, les prix des médicaments sont en partie déterminés par l’OFSP, ce qui peut dans certains cas conduire à un manque de rentabilité si l’on prend en compte les procédures d’autorisation, de production, de transport et de stockage, surtout pour le petit marché suisse. Avec la modification de la loi fédérale sur l’assurance-maladie (LAMal) du 01.01.2024, les écarts de prix entre les génériques et les biosimilaires ont encore été augmentés et peuvent désormais atteindre 70%. C’est pourquoi certains génériques, mais parfois aussi des substances actives entières, disparaissent régulièrement du marché suisse, ce qui peut avoir des répercussions considérables sur la prise en charge des patients.
La chute des prix n’est pas la seule raison des difficultés d’approvisionnement en médicaments. Les raisons peuvent varier d’un cas à l’autre. Parmi les causes possibles figurent notamment des difficultés de production, une augmentation de la demande mondiale, une pénurie de matières premières, des dysfonctionnements techniques ou des modifications des exigences réglementaires. Des facteurs externes tels que le coronavirus ou la situation géopolitique aggravent encore la situation. La collecte de signatures pour l’initiative sur la sécurité de l’approvisionnement médical est en cours en Suisse. Plus d’informations sur: https://initiative-approvisionnement.ch/initiative/
Afin de mieux faire face aux difficultés d’approvisionnement, Galexis et Sandoz ont en outre mis sur pied l’initiative Safety Stock dans le cadre d’une collaboration volontaire. Dans ce contexte, les stocks de sécurité nationaux de médicaments génériques destinés au traitement des maladies chroniques ont été fortement augmentés, permettant ainsi de combler les difficultés d’approvisionnement à court et moyen terme. Plus d’informations sur l’initiative Safety Stock: https://www.initiative-safetystock.ch/fr
Les difficultés d’approvisionnement touchent les médecins, les pharmacies, les hôpitaux et en particulier les patientes et les patients qui ont besoin de médicaments spécifiques. Par conséquent, des médicaments génériques d’autres fabricants, voire des originaux plus chers, sont prescrits ou délivrés aux personnes souffrant de troubles chroniques. Ce changement est fastidieux tant pour les médecins que pour les pharmaciennes et pharmaciens, car la tolérance doit notamment être réévaluée.
Pourquoi vaut-il la peine pour les pharmaciennes et pharmaciens et les médecins de délivrer aussi des génériques et des biosimilaires?
Outre le fait que la délivrance de génériques et de biosimilaires contribue à la réduction des coûts dans le domaine de la santé, d’autres raisons plaident en faveur de la délivrance du produit de remplacement par rapport à l’original.
Ainsi, à partir du 01.07.2024, le calcul de la part relative à la distribution des médicaments sera adapté par l’OFSP. Cela concerne les médicaments figurant sur la liste des spécialités qui peuvent être facturés par le prestataire à la caisse-maladie. Une partie de cette adaptation est l’introduction de la comparaison des substances actives, qui aura d’importantes répercussions sur le calcul de la part relative à la distribution pour les originaux ayant des génériques (ou les préparations de référence ayant des biosimilaires).
A l’avenir, les médicaments ayant la même substance active seront facturés avec une part relative à la distribution uniforme. Cette part relative à la distribution est basée sur le prix Ex-Factory moyen des génériques et s’applique également au produit original. Cela a pour effet de supprimer les incitations inopportunes à délivrer des originaux plus chers au lieu de génériques moins chers. Parallèlement, cette mesure entraînera généralement (et parfois de manière significative) une baisse de la part relative à la distribution des produits originaux. Plus sur l'adaptation de la part relative à la distribution.
D’autres mesures visant à promouvoir les génériques et les biosimilaires sont déjà en vigueur depuis le 1er janvier 2024. Ainsi, les pharmaciennes et pharmaciens peuvent désormais, avec l’accord du patient ou de la patiente, remettre le médicament biosimilaire meilleur marché au lieu du biomédicament onéreux. La quote-part pour les originaux onéreux a également été augmentée: pour les médicaments nettement plus chers que les génériques ou biosimilaires, une quote-part plus élevée de 40% (au lieu des 10% habituels) est appliquée. Par ailleurs, les prestataires sont tenus d’informer les patientes et patients lorsque la quote-part plus élevée s’applique. Ces derniers doivent être encouragés à miser davantage sur les génériques et biosimilaires moins chers.
L’utilisation systématique de génériques et de biosimilaires revêt aussi un avantage caché: la recherche pharmaceutique fait d’énormes progrès et parvient aujourd’hui à traiter des maladies rares qui ont longtemps été impossibles à traiter. De telles innovations sont toutefois liées à des coûts élevés. Pour éviter que les coûts de la santé ne deviennent incontrôlables, il est possible de réaliser des économies partout où cela n’a pas d’impact négatif au niveau du traitement. C’est l’une des grandes opportunités offertes par l’utilisation systématique des génériques et des biosimilaires.
Vous souhaitez miser davantage sur les génériques et les biosimilaires et adapter votre assortiment en conséquence? Prenez contact avec votre interlocuteur. Nous nous ferons un plaisir de vous aider.