
18. Februar 2026
17. Mai 2024
Generika und Biosimilars leisten einen wesentlichen Beitrag an Kosteneinsparungen im Gesundheitssystem. Sie tragen massgeblich dazu bei, dass neue Arzneimittel und Innovationen langfristig tragbar bleiben. Und insbesondere die Bedeutung von Biosimilars wird in Zukunft weiter steigen.
Generika und Biosimilars sind Nachfolgemedikamente von Arzneimitteln, deren Patentschutz abgelaufen ist. Der Unterschied zwischen Generika und Biosimilars liegt darin, dass sich Generika auf ein chemisch hergestelltes Originalpräparat und Biosimilars auf ein biologisch hergestelltes Referenzpräparat beziehen
Sowohl Generika wie auch Biosimilars sind nach den gleichen strengen Qualitäts-, Sicherheits- und Wirksamkeitsstandards durch die Zulassungsbehörde Swissmedic zugelassen, die auch für alle anderen Medikamente gelten.
Damit ein Generikum zugelassen wird, muss unter anderem die Bioäquivalenz des Generikums nachgewiesen werden. Das heisst, die Menge und Geschwindigkeit, mit welcher der Körper den Wirkstoff aufnimmt, muss dem Original innerhalb enger Grenzen entsprechen. Hersteller müssen dies durch Untersuchungen nachweisen. Durch dieses Zulassungsverfahren ist sichergestellt, dass das Generikum die gleiche Qualität und Sicherheit besitzt. Zusätzlich muss der Hersteller nachweisen, dass die Produktion den Qualitätsstandards entspricht, was durch Stichproben und Betriebsinspektionen geprüft wird. Generika sind also bezüglich Qualität und Sicherheit absolut gleichwertig mit den Originalprodukten.
Auch Biosimilars sind nach den gleichen strengen Qualitäts-, Sicherheits- und Wirksamkeitsstandards zugelassen, die für alle anderen Medikamente gelten. Bei Biosimilars muss die Ähnlichkeit (similar = ähnlich) zum Referenzprodukt nachgewiesen werden. Entscheidende Faktoren sind Qualität, biologische Aktivität, Sicherheit und Wirksamkeit. Die Zulassung von Biosimilars stützt sich vor allem auf vergleichende analytische Studien. Die Hersteller müssen belegen, dass das Biosimilar einem «Referenzpräparat bezüglich Struktur, pharmazeutischer Qualität, biologischer Aktivität, Wirksamkeit, Sicherheit und Immunogenität genügend ähnlich ist, um relevante klinische Unterschiede mit genügender Sicherheit auszuschliessen». Dazu werden die neusten analytischen und biotechnologischen Methoden verwendet, um die Vergleichbarkeit mit den Referenzprodukten aufzuzeigen.
Quelle: intergenerika.ch, biosimilar.ch
Was sind die Vorteile von Generika und Biosimilars?
Generika und Biosimilars leisten einen wesentlichen Beitrag an Kosteneinsparungen im Gesundheitssystem, da sie deutlich günstiger sind als die jeweiligen Original- bzw. Referenzpräparate. Dies ist möglich, da Generika-Hersteller geringere Kosten für Forschung und Entwicklung haben. Durch den Einsatz von Generika können Gesundheitssysteme erhebliche Einsparungen erzielen, insbesondere wenn es um langfristige Verschreibungen für chronische Krankheiten geht.
Allerdings hinkt die Schweiz gerade bei den Biosimilars im europäischen Vergleich hinterher, obwohl moderne Biopharmazeutika Behandlungen und Heilungen in Therapiegebieten ermöglichen, in welchen es bisher kaum Möglichkeiten gab. So schaffen sie für die betroffenen Patientinnen neue Chancen auf eine Verbesserung ihrer Lebensqualität. Biosimilars sind dabei eine Chance, Kosten zu senken, ohne die Patientensicherheit, die Versorgungssicherheit oder den Zugang zu wichtigen Therapien zu gefährden. In diesem Zusammenhang sind Biosimilars unerlässlich, um teure Innovationen im Bereich der biologischen Wirkstoffe überhaupt tragbar zu machen. Allerdings wird der noch tiefe Biosimilar-Anteil in der Schweiz deren therapeutischem Stellenwert nicht gerecht. Darum setzt sich auch das BAG in letzter Zeit mit verschiedenen Massnahmen verstärkt für die Förderung von Biosimilars ein.
Im grössten Pharma- und Non-Pharma-Sortiment der Schweiz finden Sie bei Galexis alle hierzulande registrierten RX- und OTC-Arzneimittel, darunter eine steigende Zahl von Biosimilars.
Generika weisen, neben den kostenbedingten Vorteilen, weitere positive Eigenschaften auf, die sie von Originalpräparaten abheben. So enthalten Generika nur bewährte Wirkstoffe, die aufgrund langjähriger therapeutischer Erfahrung bestens bekannt und dokumentiert sind.
Ausserdem sind Generika im Vergleich zu ihren Referenzprodukten, die vor 10 oder mehr Jahren entwickelt wurden, meist modernere Präparate, da sich die technischen Standards in der Entwicklung und Herstellung teilweise signifikant weiterentwickelt haben. Unter anderem ermöglichen verbesserte galenische Formen die Vermeidung von Zusatzstoffen wie Konservierungsmitteln. So können Generika oftmals in kundenfreundlicheren Darreichungsformen angeboten werden, beispielsweise in als teilbare Tablette oder auch vegan oder laktosefrei.
Wie ist der Generika- und Biosimilarsmarkt aufgebaut?
Grundsätzlich ist der Medikamentenmarkt in zwei Bereiche aufgeteilt – in den Markt der patentgeschützten und in den patentfreien Markt. Der patentgeschützte Markt umfasst Innovationen, der patentfreie Markt umfasst Nachfolgemedikamente (Generika und Biosimiliars) sowie patentfreie Originale. Letzterer wird auch als substitutionsfähiger Markt bezeichnet, also der Teil des Medikamentenmarkts, in welchem eine Substitution des Original- resp. Referenzpräparats durch das entsprechende Generikum bzw. Biosimilar möglich ist. Der patentgeschützte und der patentfreie Markt nehmen gemessen am Umsatz je rund die Hälfte des Gesamtmarkts ein (Abb. 1), gemessen an Anzahl abgegebener Packungen macht der patentfreie Markt über 90% aus (Abb. 2).
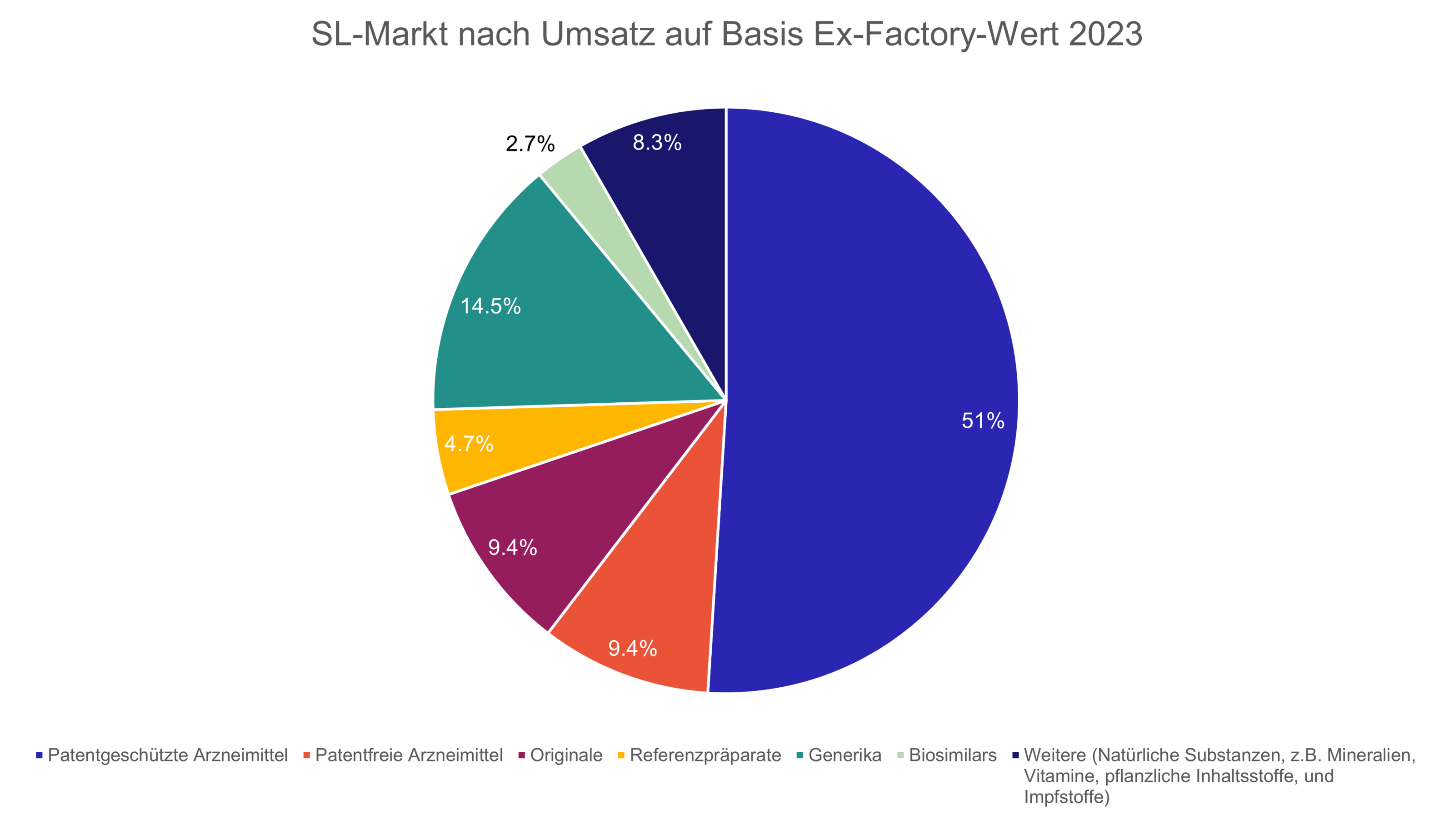
Die Anzahl Generika und Biosimilars, die grundsätzlich verfügbar sein könnten, hängt also direkt mit der Anzahl der Originalmedikamente zusammen, welche entwickelt werden und deren Patente irgendwann ablaufen. Je grösser der Anteil von Generika im innerhalb des substitutionsfähigen Markts gegenüber Originalen ist, desto mehr vom Sparpotenzial wird genutzt. Vergleicht man beispielsweise Generika mit Originalprodukten für das Jahr 2023, so werden sowohl gemessen am Umsatz (14.5% vs. 9.4% vom Gesamtmarkt, Abb. 1) wie auch in Packungen (31.2% vs. 17.6% vom Gesamtmarkt, Abb. 2) mehr Generika abgegeben. Die verbleibenden 9.4% (in Umsatz) bzw. 17.6% (in Packungen) bilden das theoretische Substitutionspotenzial durch Generika ab.
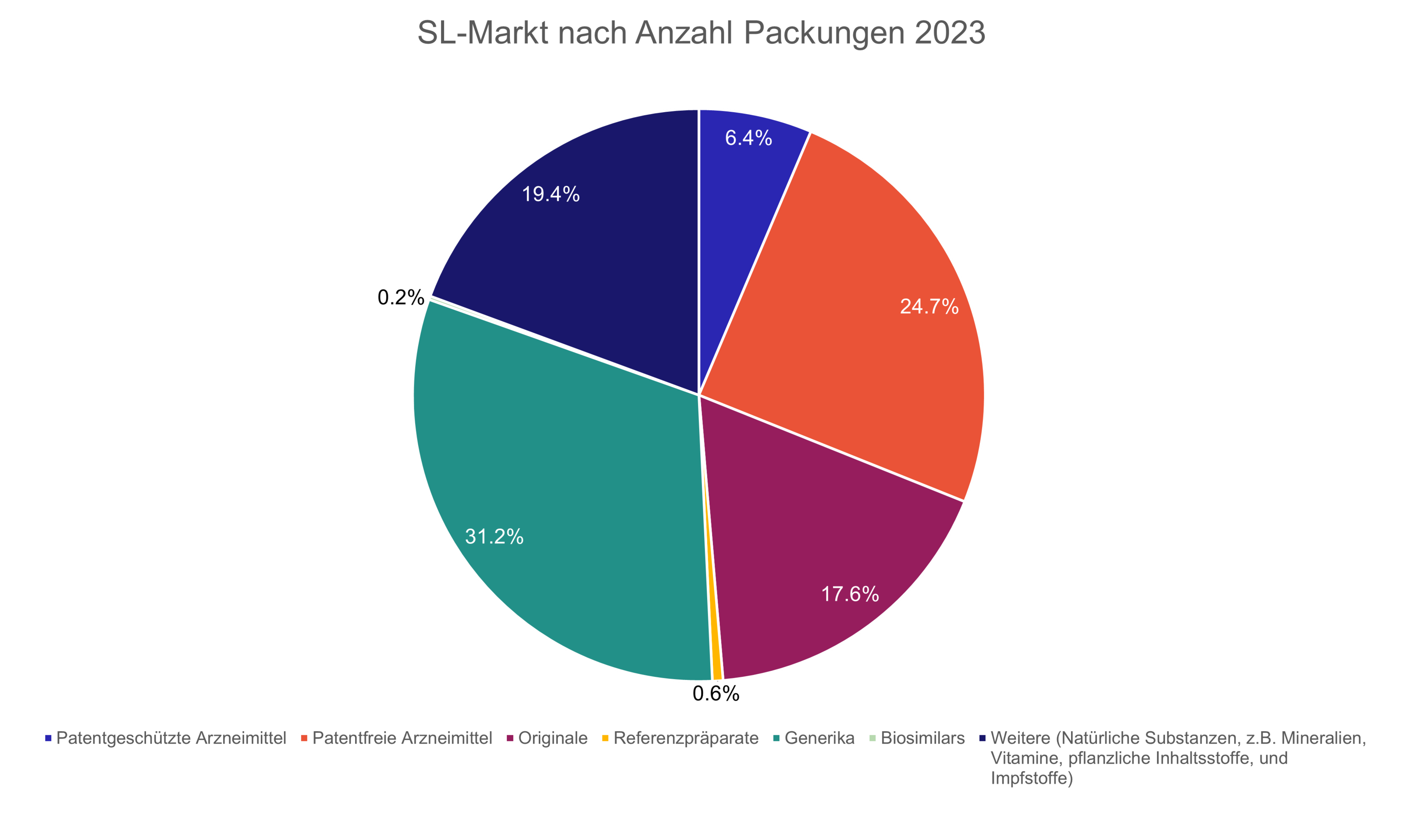
Insbesondere bei Biosimilars besteht jedoch grosses Potential für weitere Einsparungen, was auch in den Zahlen zu sehen ist. So wurden 2023 sowohl in Umsatz (4.3% vs. 2.7% vom Gesamtmarkt, Abb. 1) wie auch in Packungen (0.6% vs. 0.2% vom Gesamtmarkt, Abb. 2) mehr Referenzprodukte also Biosimilars abgegeben. Dies ist insofern besonders relevant, weil in den nächsten Jahren viele Patente von biologischen Arzneimitteln ablaufen werden (siehe auch Abschnitt «Verschiebung vom Generikamarkt zum Biosimilarsmarkt»).
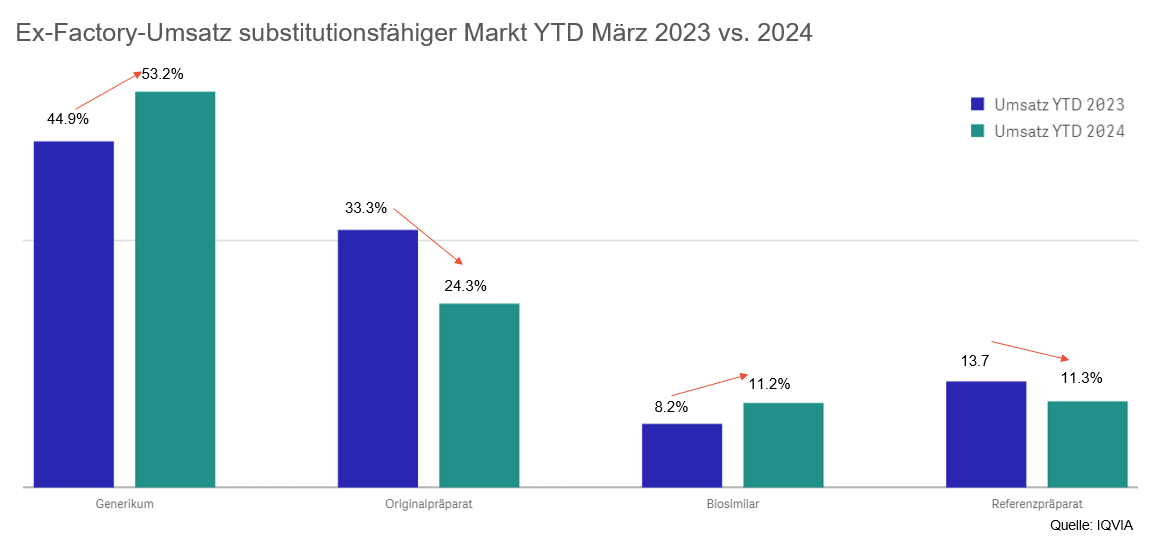
Trotzdem zeigt sich bereits in den ersten Monaten des Jahrs 2024 eine starke Marktdynamik innerhalb des substitutionsfähigen Markts, was auf die verschiedenen Massnahmen des BAG zurückzuführen ist, die am 1. Januar in Kraft getreten sind und am 1. Juli noch in Kraft treten werden (siehe dazu auch Abschnitt «Warum lohnt es sich?»). So sind die Umsätze bei Generika und Biosimilars teils deutlich gestiegen, während der Einsatz von Originalen bzw. Referenzprodukten zurückgegangen ist. Es ist anzunehmen, dass sich dieser Trend im Lauf des Jahres weiter fortsetzen wird.
Verschiebung vom Generikamarkt zum Biosimilarsmarkt
Lange Zeit war der substitutionsfähige Markt praktisch ein reiner Generikamarkt. Noch bis vor kurzem lag der Umsatzanteil an auslaufenden Patenten bei chemisch hergestellten Wirkstoffen deutlich höher als jener der biologisch hergestellten Wirkstoffe. Der substitutionsfähige Markt bei Arzneimitteln unterliegt aber einer starken Dynamik, sodass sich die Anteile von Generika und Biosimilars in den kommenden Jahren deutlich verschieben werden. Der Anteil an Biologika, deren Patent in den kommenden Jahren auslaufen wird, ist massiv gestiegen und wird noch weiter steigen, da biologische Arzneimittel einen immer grösseren Stellenwert in der Behandlung und Heilung von Krankheiten einnehmen, für die es früher keine Behandlungsmöglichkeiten gab. Bereits heute übersteigt der weltweite Umsatz von neu patentabgelaufenen Biologika den Umsatz von neu patentabgelaufenen Synthetika (Abb. 4).
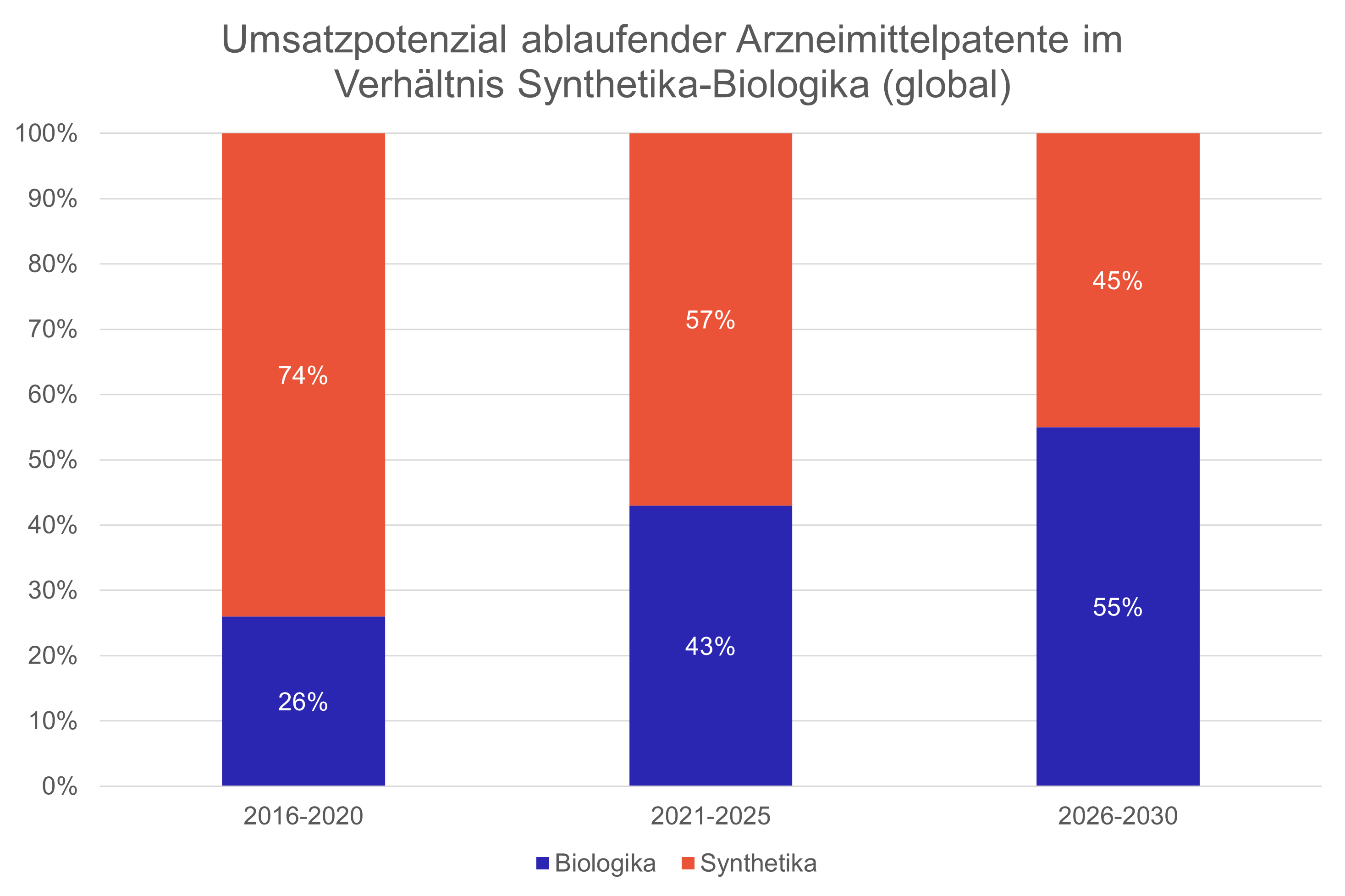
Entsprechend wird die Bedeutung von Biosimilars weiter zunehmen, um die Kosten im Gesundheitssystem unter Kontrolle zu halten, ohne die Patientensicherheit, die Versorgungssicherheit oder den Zugang zu wichtigen Therapien zu gefährden. Gleichzeitig trägt die Entwicklung von Biosimilars auch dazu bei, dass solche kostenintensiven biologischen Arzneimittel überhaupt tragbar sind. Darum ist es wichtig, sich frühzeitig auf diese Entwicklung einzustellen.
Was sind die Herausforderungen im Generika- und Biosimilarsmarkt?
Generika und Biosimilars – obwohl bereits deutlich günstiger als Original- resp. Referenzprodukte – sind einem starken Kostendruck ausgesetzt. Im stark regulierten Schweizer Gesundheitsmarkt werden die Medikamentenpreise vom BAG mitbestimmt, was unter Umständen dazu führt, dass sich Zulassung, Produktion, Transport und Lagerung – gerade für den kleinen Schweizer Markt – nicht mehr lohnen. Mit der Änderung des Krankenversicherungsgesetztes (KVG) vom 01.01.2024 wurden die Preisabstände von Generika und Biosimilars noch einmal weiter erhöht und können nun bis zu 70% betragen. Deshalb verschwinden immer wieder einzelne Generika, teilweise aber auch ganze Wirkstoffe vom Schweizer Markt, was wiederum massive Auswirkungen auf die Patientenversorgung haben kann.
Der Preiszerfall ist nicht der einzige Grund für Lieferengpässe bei Arzneimitteln. Diese können sich von Fall zu Fall unterscheiden. Mögliche Ursachen können etwa Produktionsengpässe, eine steigende weltweite Nachfrage, Rohstoffknappheit, technische Störungen oder Änderungen der behördlichen Anforderungen sein. Verschärfend wirken externe Faktoren wie Corona oder die geopolitische Situation. Aktuell läuft in der Schweiz die Unterschriftensammlung für die Initiative zur medizinischen Versorgungssicherheit. Mehr Infos unter: https://versorgungsinitiative.ch/initiative/
Um Lieferengpässen besser begegnen zu können, haben Galexis und Sandoz zudem in freiwilliger Zusammenarbeit die Initiative Safety Stock ins Leben gerufen. Im Zuge dessen wurden die nationalen Sicherheitsbestände von generischen Medikamenten zur Behandlung chronischer Krankheiten stark erhöht, was kurz- und mittelfristige Lieferengpässe überbrücken kann. Mehr Informationen zur Initiative Safety Stock: https://www.initiative-safetystock.ch/
Versorgungsengpässe betreffen Ärzte, Apotheken, Spitäler und insbesondere Patientinnen und Patienten, die auf die notwendigen Medikamente angewiesen sind. In der Folge werden an Personen mit chronischen Leiden alternative Generika anderer Hersteller oder gar teurere Originale verordnet oder abgegeben. Diese Umstellung ist sowohl für Ärztinnen und Ärzte als auch Apothekerinnen und Apotheker mit Aufwand verbunden, da unter anderem z.B. die Verträglichkeit neu ermittelt werden muss.
Warum lohnt es sich auch für Apotheker und Ärzte, Generika und Biosimilars abzugeben?
Neben der Tatsache, dass die Abgabe von Generika und Biosimilars zur Kostensenkung im Gesundheitswesen beiträgt, gibt es weitere Gründe, die für die Abgabe des Nachfolgeprodukts gegenüber dem Original sprechen.
So wird ab dem 01.07.2024 die Berechnung des Vertriebsanteils für Arzneimittel durch das BAG angepasst. Dies betrifft Arzneimittel auf der Spezialitätenliste, welche vom Leistungserbringer mit der Krankenkasse abgerechnet werden können. Teil dieser Anpassung ist die Einführung des sogenannten Wirkstoffvergleichs, welcher grosse Auswirkungen auf die Berechnung des Vertriebsanteils bei Originalen mit Generika (resp. Referenzpräparaten mit Biosimilars) haben wird.
Künftig werden wirkstoffgleiche Arzneimittel mit einem einheitlichen Vertriebsanteil abgerechnet. Dieser Vertriebsanteil basiert auf dem durchschnittlichen Ex-Factory-Preis der Generika und gilt dann jedoch auch für das Originalprodukt. Das hat zur Folge, dass Fehlanreize, teurere Originale statt günstigere Generika abzugeben, behoben werden. Gleichzeitig wird durch diese Massnahme der Vertriebsanteil von Originalprodukten in der Regel (und zum Teil deutlich) sinken. Mehr zur Anpassung des Vertriebsanteils.
Bereits seit dem 1. Januar 2024 gültig sind weitere Massnahmen zur Stärkung von Generika und Biosimilars. So können Apothekerinnen und Apotheker neu mit dem Einverständnis des Patienten statt dem teuren Biologika das günstigere Biosimilar abgeben. Auch der Selbstbehalt für teure Originale wurde erhöht. Bei Arzneimitteln, die im Vergleich zu günstigen Generika oder Biosimilars wesentlich teurer sind, kommt ein erhöhter Selbstbehalt von 40% (statt der üblichen 10%) zum Tragen. Ausserdem sind Leistungserbringer verpflichtet, Patienten darauf hinzuweisen, wenn der erhöhte Selbstbehalt gilt. So sollen Patienten motiviert werden, vermehrt auf die günstigeren Generika und Biosimilars zu setzen.
Der konsequente Einsatz von Generika und Biosimilar hat auch einen versteckten Nutzen: Die Arzneimittelforschung macht enorme Fortschritte und schafft es heute, auch seltene Krankheiten zu behandeln, bei denen dies lange unmöglich war. Doch solche Innovationen sind mit hohen Kosten verbunden. Damit die Gesundheitskosten nicht aus dem Ruder laufen, kann dort gespart werden, wo keine Nachteile in der Therapie entstehen. Das ist eine der grossen Chancen, welche sich beim konsequenten Einsatz von Generika und Biosimilars ergeben.
Sie möchten vermehrt auf Generika und Biosimilars setzen und Ihr Sortiment entsprechend anpassen? Nehmen Sie mit Ihrer Ansprechperson Kontakt auf. Wir unterstützen Sie gerne.